Die Atmosphäre
Als Luft bezeichnet man das Gas, welches uns auf der Erdoberfläche umgibt und aufgrund seiner Zusammensetzung wichtigste Voraussetzung für ein Leben auf der Erde ist. Die Luftschicht, die sogenannte Erdatmosphäre, ist mehrere 100 km dick, wobei der Luftdruck in 50 km Höhe weniger als 1/1000 des Luftdrucks an der Erdoberfläche beträgt. Das Wettergeschehen spielt sich in der Lufthülle unterhalb einer Höhe von 15 km ab.Zusammensetzung der Luft
Die Luft ist (wie ihre Einzelbestandteile) ein unsichtbares, geruch- und geschmackloses Gasgemisch, das aus mehreren einzelnen Gasen mit unterschiedlichen physikalischen und chemischen Eigenschaften zusammengesetzt ist. Die beiden Hauptbestandteile trockener Luft sind (molekularer) Stickstoff (78 %) und (molekularer) Sauerstoff (21 %). Der Rest besteht aus Argon, Kohlendioxid, Neon und Helium. Feuchte Luft kann bis zu 4 % Wasserdampf enthalten. Für Wetterphänomene ist dieser Wasserdampf von großer Bedeutung.Auf Meeresniveau beträgt die Dichte der Luft etwa 1,293 g/Liter, mit anderen Worten: ein Liter Luft wiegt etwa 1,3 g bzw. ein m³ Luft wiegt 1,3 kg. Mit wachsender Entfernung von der Erde nimmt die Dichte der Luft schnell ab, die Atemluft wird „dünner“.
Die größten Veränderungen in der Zusammensetzung der Luft ergeben sich seit Beginn der Industrialisierung Mitte des 18. Jahrhunderts durch den zunehmenden Anteil des CO2. CO2 trägt als Treibhausgas (neben anderen Gasen wie Methan, Distickstoffoxid, Fluorkohlenwasserstoffe, Schwefelhexafluorid) wesentlich zum Treibhauseffekt und damit zur globalen Erderwärmung bei. Der Einfluss des CO2 wird gerade in den aktuellen internationalen Diskussionen und Gremien um den Klimaschutz deutlich.
Luftfeuchtigkeit
Unsere Umgebungsluft ist nicht völlig trocken, sondern enthält je nach Standort 0 - 7% Wasserdampf. Wasser aus Meeren, Seen, Flüssen aber auch von Tieren und Pflanzen verdunstet, d.h. es geht vom flüssigen in den gasförmigen Zustand (Wasserdampf) über. Wasserdampf kann aber nur bis zu einer bestimmten Menge von der Luft aufgenommen werden. Bei einem höheren Anteil beginnt der Wasserdampf zu kondensieren: es bilden sich Nebel (Wolken) oder Tautropfen. Diese sogenannte Sättigungsmenge steht dabei in direktem Zusammenhang mit der Lufttemperatur: je wärmer die Luft ist, desto mehr Wasserdampf kann sie aufnehmen und desto höher ist auch der Grad der Feuchtigkeit, dessen Wert in Prozent angegeben wird. 100% Feuchtigkeit bedeutet also, dass die Luft ihrer Temperatur entsprechend die maximale Menge an Wasserdampf enthält. Man spricht auch von der absoluten Luftfeuchtigkeit. Die relative Feuchtigkeit (z.B. 65%) gibt dabei den Grad der Sättigung an. Die Luftfeuchtigkeit wird mit einem sogenannten Hygrometer bestimmt. Für das Wohlbefinden der Menschen spielt sie eine erhebliche Rolle. Wenn es schwül ist, d.h. wenn die Luft bereits viel Feuchtigkeit enthält, kann unser Schweiß auf der Haut nicht schnell genug verdunsten. Die in unserem Körper entstandene Wärmeenergie kann dann nicht ausreichend schnell durch Verdunstung abgeführt werden.Luft nimmt Raum ein
Die Luft ist zwar unsichtbar, beansprucht aber trotzdem Raum. Die Luft besteht aus verschiedenen kleinen Gasteilchen (Atome und Moleküle), die nicht aneinander gebunden sind und sich mit hoher Geschwindigkeit - bei Zimmertemperatur bis 500 m/s – in relativ großem Abstand frei bewegen und dabei fortgesetzt miteinander zusammenstoßen. Sie füllen jeden ihnen zur Verfügung stehenden Raum vollständig aus. In einem geschlossenen System prallen die Gasteilchen nicht nur aufeinander, sondern auch auf die Begrenzungswände und üben dadurch eine Druckkraft auf sie aus. Wird die Anzahl der Gasteilchen bei gleichbleibendem Volumen erhöht, wodurch mehr Teilchen aufeinander und gegen die Wände prallen, steigt auch der Druck im Gas.Luft kann komprimiert werden
Die Luft ist, wie alle anderen Gase auch, aufgrund des relativ großen Abstandes der Luftteilchen untereinander und im Gegensatz zu den Flüssigkeiten und festen Körpern bis zu einem gewissen Grad komprimierbar. Diese Erfahrung macht man, wenn man auf den Kolben einer mit Luft gefüllten Spritze (ohne Nadel) oder eine Luftpumpe Druck ausübt und dabei die Öffnung mit einem Finger zuhält. Durch die Komprimierung wird das Volumen des Systems bei gleichbleibender Anzahl an Gasteilchen verkleinert. Auf der Molekularebene bedeutet dies, dass auf eine Wandfläche nun mehr Teilchen prallen, wodurch sich die Druckkraft auf die Wand erhöht. Verringert man die äußere Kraft, mit der der Kolben in die Spritze hineingedrückt wird, schiebt die unter zunächst höherem Druck stehende Luft den Kolben wieder ein Stück heraus. So kann man sagen, dass Luft elastisch ist: ein leicht zusammengedrückter Luftballon dehnt sich wieder zu seiner ursprünglichen Gestalt aus.Gasgesetze
Die physikalischen Verhältnisse und Eigenschaften eines gasförmigen Zustands lassen sich durch ein allgemein gültiges – für ideale Gase besonders einfaches – Gasgesetz beschreiben, das eine Beziehung zwischen den Zustandsgrößen Druck (p), Temperatur (T), Volumen (V) und Teilchenzahl (N) herstellt.Ideale Gase
Bei idealen Gasen wird angenommen, dass ihre Teilchen kein Eigenvolumen besitzen. Sie üben untereinander keine Kräfte aus (außer bei direkten Zusammenstößen). Luft kann hinunter bis zu Temperaturen von mehr als -100°C als ein ideales Gas angesehen werden.Die Zustandsgleichung für ein ideales Gas lautet:
p V = N k T (k ist eine Konstante)
Aus dieser Gleichung lassen sich zahlreiche Schlussfolgerungen ziehen. Schließt man z.B. ein Gas in ein festes Gefäß ein, so dass sich das Volumen und die Teilchenzahl nicht ändern können, und erhöht man die Temperatur, dann erhöht sich auch der Druck. Vergrößert man bei konstanter Temperatur und gleichbleibender Teilchenzahl das Volumen, dann sinkt der Druck. Erwärmt man ein Gas bei konstantem Druck (z.B. bei Atmosphärendruck), dann vergrößert sich nach der Gasgleichung das Volumen. Damit wird die Dichte des Gases kleiner und es gibt einen Auftrieb, wenn die erwärmte Luft von kälterer Luft umgeben ist.
Aus der Gasgleichung nicht direkt ablesbar ist es, dass sich im allgemeinen Fall sowohl der Gasdruck als auch seine Temperatur erhöhen, wenn man das Volumen verkleinert. Das stellt man z.B. fest, wenn man einen Fahrradreifen aufpumpt: Nach einigen Pumpenstößen hat sich die Luftpumpe erwärmt. Durch das Komprimieren erhöht man den Energiegehalt des Gases, und dies zeigt sich durch eine Temperaturerhöhung.
Reale Gase
Bei den sogenannten realen Gasen wird berücksichtig, dass die Teilchen ein Eigenvolumen besitzen und es zwischen den Teilchen anziehende und abstoßende Kräfte gibt (ohne anziehende Kräfte könnte ein Gas z.B. nicht kondensieren).Luftdruck
Die Luft eines Volumens von einem Liter hat eine Masse von ca. 1,3 g. Da die Luft von der Erde angezogen wird (sonst hätte sich die Luft schon seit langem in den Weltraum verflüchtigt) wird auf die Luft eine Gewichtskraft ausgeübt. Da die Luftschicht über der Erdoberfläche einige Kilometer dick ist, wird eine enorme Druckkraft von der Luft auf alle Flächen ausgeübt. Der Luftdruck ist also ein Schweredruck, der durch das Gewicht der Luftsäule über einer bestimmten Fläche zustande kommt.
Otto von Guericke, der im 17. Jahrhundert auf diese physikalische Besonderheit der Luft in seinem Experiment der Magdeburger Halbkugeln stieß, versuchte den Luftdruck mit Hilfe einer Wassersäule zu ermitteln und stellte fest, dass der auf uns herrschende Luftdruck so groß ist, dass er eine Wassersäule von 10m Höhe halten kann und das Ausfließen des Wassers verhindert. Dadurch, dass die Dichte und damit das Gewicht der Luft nach oben hin abnehmen, ist dementsprechend auch der Luftdruck in hohen Lagen niedriger als in tiefen Lagen. Als Normaldruck wird der Druck, der auf Meereshöhe herrscht, verstanden. Der Druck ist definiert durch die Kraft, die auf eine bestimmte Fläche wirkt und wird in der Einheit Pascal angegeben:
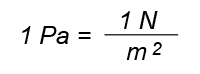
Da dies ein sehr kleiner Wert im Vergleich zum Luftdruck ist, wird meist die Einheit bar verwendet. Diese entspricht 100 000 Pascal. Der Atmosphärendruck liegt bei etwa 1 bar.
Beim Trinken mit einem Strohhalm sorgen wir durch die Vergrößerung des Brustkorbs und damit des Lungenvolumens dafür, dass der Luftdruck in unserem Mund sinkt und kleiner als der Atmosphärendruck wird. Das daraus resultierende Ungleichgewicht zwischen äußerem und innerem Luftdruck führt dazu, dass eine Kraft auf die Oberfläche der Flüssigkeit wirkt und diese dadurch in den Strohhalm und in unseren Mund gedrückt wird. In diesem Sinne ist es nicht sinnvoll, von Saugen zu sprechen, da es auf die Druckdifferenz ankommt.
In der Natur beobachtet man das Phänomen des Druckausgleichs bei der Entstehung von Wind (bewegte Luft). Dieser entsteht, wenn in verschiedenen Gebieten unterschiedliche Luftdrücke herrschen. Luft strömt von Gebieten mit höherem Druck zu Gebieten mit niedrigerem Druck. Je größer der Druckunterschied ist, desto stärker ist auch der Wind.
Luftwiderstand
Bewegt sich ein Körper durch die Luft (bzw. relativ zur Luft), dann muss die Luft vor dem Körper weggeschoben werden. Da Luft eine Masse hat, muss dafür eine Kraft auf die Luft ausgeübt werden, und die Luft übt deshalb gleichzeitig eine bremsende Kraft auf den Körper aus (Wechselwirkungsprinzip). Diese Kraft auf den Körper wird Luftwiderstand genannt. Je größer die Oberfläche und die Geschwindigkeit des sich bewegenden Gegenstandes sind, desto größer ist der Luftwiderstand. Außerdem hängt er von der geometrischen Form ab (angegeben durch den so genannten cw-Wert). Den Luftwiderstand spürt man deutlich beim Fahrradfahren mit Gegenwind. Die Bremswirkung eines Fallschirms ist ebenfalls auf den Luftwiderstand zurückzuführen.Auftrieb
Erwärmt sich Luft, z.B. über einem von der Sonne beschienenen Felsen oder über einer Flamme, dann dehnt sie sich aus. Damit nimmt ihre Dichte ab, und die erwärmte Luft erfährt einen Auftrieb, wenn sie von kälterer Luft umgeben ist. Dieser Auftrieb kann so stark sein, dass ein Heißluftballon mit angehängter Gondel nach oben getragen werden kann.Weshalb ein Flugzeug fliegen kann, ist nicht einfach zu erklären. Eine sehr vereinfachte Erklärung lautet: Die Luft strömt gegen den schräg stehenden Flügel und wird dadurch nach unten abgelenkt. Der Flügel übt also eine Kraft auf die Luft nach unten aus. Gleichzeitig übt (nach dem Wechselwirkungsprinzip) die Luft eine Kraft auf den Flugzeugflügel nach oben aus. Ist diese Kraft groß genug, bleibt das Flugzeug in der Luft.
Atmung
Für uns Lebewesen ist die Luft, die wir einatmen lebensnotwendig, da sie den für uns nötigen Sauerstoff enthält. Beim Ausatmen wird Kohlendioxid an die Außenluft abgegeben. Der in der Luft enthaltene Sauerstoff wird beim Atmen nicht vollständig verbraucht, in der ausgeatmeten Luft ist noch etwa 16% Sauerstoff enthalten. Das Kohlendioxid in der ausgeatmeten Luft hat einen Anteil von 4%. Auch bei der Atmung spielt der Luftdruck eine erhebliche Rolle. Beim Einatmen senkt sich das Zwerchfell (die untere Begrenzung des Brustkorbs) und die Rippen werden gehoben, wodurch sich der Brustraum und damit das Lungenvolumen vergrößern. Dadurch sinkt der Luftdruck in den Lungen. Der Druckunterschied zwischen außen und innen führt nun dazu, dass Luft von außen nach innen in die Lungenbläschen strömt. Beim Ausatmen findet der umgekehrte Vorgang statt. Das Zwerchfell wird angehoben, Brustraum und Lungenvolumen verkleinern sich. Es herrscht nun innen ein größerer Luftdruck als außen, wodurch die Luft nach außen strömt.Weiterführende Informationen zur Zusammensetzung der Luft
Der Stickstoff
Das chemische Symbol für das Element Stickstoff lautet N. Er ist in seiner natürlichen molekularen Form (N2) durch seine hohe Bindungsenergie bei niedrigen Temperaturen ein äußerst reaktionsträges Gas. Erst bei Temperaturen ab ca. 5000° C geht er mit Sauerstoff eine Verbindung, das Stickstoffdioxid, ein. Diese Eigenschaft als chemisch träges Gas wird vor allem in der Technik ausgenutzt, wo der Stickstoff als Schutzgas verwendet wird und dabei die Aufgabe hat, Luft aus der Atmosphäre zu verdrängen. Dieses Verfahren wird am häufigsten in Verpackungen von Lebensmitteln verwendet, damit diese nicht mit Sauerstoff reagieren können oder sie vor Bakterien aus der Luft geschützt werden. Die Kühlwirkung von Stickstoff durch seine niedrige Siedetemperatur von -196° C wird z.B. in Kühlwägen eingesetzt.Der Sauerstoff
Wie der Stickstoff so liegt auch der Sauerstoff (O) als zweiatomiges Molekül vor (O2). Er ist das am häufigsten in der Natur vorkommende Element. Neben seinem Anteil in der Luft ist er zu 47,7% in der Erdrinde und zu 85,5% in Wasser gebunden. Der Sauerstoff als wichtigstes Oxidationsmittel in der Atmosphäre ist selbst nicht brennbar. Er erhält aber den Verbrennungsvorgang und wird für die Atmung aller Lebewesen benötigt. In der Natur wird er über die Photosynthese der Pflanzen gebildet, wo unter Lichtzufuhr aus Kohlendioxid und Wasser Zucker und Sauerstoff entstehen. In der Medizin wird er vor allem in Beatmungsgeräten eingesetzt. In der Chemie wird der Sauerstoff durch die sogenannte Glimmspanprobe nachgewiesen (taucht man einen glühenden Holzspan in eine Sauerstoff enthaltende Atmosphäre, beginnt dieser zu brennen).Das Kohlenstoffdioxid
Auch wenn das Kohlenstoffdioxid nur zu einem geringen Anteil in der Luft enthalten ist, soll es hier aufgrund seiner Bedeutung für Klima und Lebewesen mit aufgeführt werden. Im Gegensatz zum Sauerstoff verhindert das Kohlenstoffdioxid (CO2) durch „Ersticken“ den Verbrennungsvorgang. In der Natur gilt es als wichtigster Kohlenstofflieferant für die Photosynthese der Pflanzen und deren Wachstum. Bekannt ist es ebenso unter dem Namen „Trockeneis“ (festes CO2 verdampft bei Normaldruck, ohne dabei flüssig zu werden). Bei der Atmung geben Lebewesen beim Ausatmen CO2 an die Luft ab. In der Chemie wird Kohlenstoffdioxid durch die Trübung von Kalkwasser (Calciumhydroxid-Lösung) bei dessen Einleitung nachgewiesen. Da es schwerer als Luft ist, lässt es sich wie Wasser von einem Glas in ein anderes umschütten. Dieses Phänomen wird häufig in einem Schülerexperiment verwendet, bei dem aus Backpulver (Natriumhydrogencarbonat) und Essig (Essigsäure) CO2 hergestellt wird und dieses wie von „Geisterhand“ – es ist bekanntlich unsichtbar – beim Umschütten des Glases eine Kerzenflamme erlischt. Auch in der Industrie erhält man CO2 durch Reaktion von Carbonaten mit Säuren oder durch die Verbrennung mit Koks.Luftverschmutzung
Unter Luftverschmutzung oder Luftverunreinigung wird nach dem Bundesimmisionsschutzgesetz die Veränderung der natürlichen Zusammensetzung der Luft verstanden, insbesondere durch Schadstoffe wie Schwefeldioxid (saurer Regen), Staub, Ozon, Stickoxide, Kohlendioxid, Kohlenmonoxid, Ruß, u.v.m., die vor allem durch Verkehr, Industrie, Landwirtschaft, Kraftwerke und Müllverbrennung entstehen und in die Erdatmosphäre gelangen und durch ihre chemischen und physikalischen Eigenschaften Mensch, Umwelt und das ökologische Gleichgewicht in der Natur schädigen (www.umweltlexikon-online.de/fp/archiv/RUBluft/Luft.php, www.umweltdatenbank.de/lexikon/atmosphaere.htm).Durch gesetzliche Vorgaben zur Luftreinhaltung ist die lokale Luftverschmutzung in den meisten Industrieländern in den letzten Jahrzehnten stark zurückgegangen, in manchen Ländern stellt sie jedoch immer noch ein erhebliches Problem dar (z.B. Dritte Welt, Schwellenländer). Zu vermerken ist jedoch der aktuell vermehrte Ausstoß von Treibhausgasen (wie das Kohlenstoffdioxid) die zu einer akuten Belastung beitragen.
Druckversionen
als doc-Datei (61 KB)
als pdf-Datei (104 KB)

